6517B靜電計變型記
——6517B-OI兩電極電位測量變身酸度計
 | 電位測量需要測量兩個電極之間的電位,一般是工作電極和基準電極。在本文中使用海洋儀器推出的靜電計6517B-OI測量電位差。6517B-OI具有高阻電壓表功能,因此任何電流流動都可以忽略不計(i=0)。電位測量用于pH測量及使用離子選擇電極進行的電壓測量等應用。這些電位測量通常使用兩個電極和一個靜電計進行。 |
酸度計也稱為pH計,一般用來測量溶液中氫離子的活度,是6517B-OI典型的兩電極電位測量原理的應用,酸度計在實驗室中用來測定溶液的H+濃度/酸堿度的儀器。許多化學反應和實驗條件都受溶液酸堿特性的影響,對酸堿條件要求不高的實驗,溶液的酸堿度可以用pH試紙來測量,但對酸堿條件要求高、pH值對測定結果有影響的實驗,需要用酸度計來測量。現代酸度計具有:結構簡單,操作方便,測量準確和自動化程度高的優點。
酸度計的工作原理和結構pH值的定義: pH=-log H+
6517B-OI作為酸度計使用時,按其儀器應用化分為電化學分析儀器,基于電位分析法的原理測量氫離子濃度。電位分析法是根據測量化學原電池的電極電位E,用能斯特方程求得溶液中待測離子的濃度。所謂化學原電池是一種借助氧化還原反應將化學能轉變為電能的裝置,由正負兩個電極組成,中間由KCl鹽橋溝通電路,當用導線將原電池的兩級連接起來時,便產生了電流,我們通過6517B-OI的高阻電壓表功能,測量兩電極之間的電極電位,高阻的電壓表可防止兩電極導通極化,很好的保障了電極的正常工作,將所得數據代入能斯特方程式,即可求得溶液中H+離子濃度:
![]()
式中:E為電極電位,ax為離子濃度酸度計的結構是由電極和電計兩部分組成。電極部分是基于化學原電池的原理設計而成,由工作電極和參比電極組成,在測試過程中將兩電極連接到6517B-OI,通過儀器的精細電壓測量功能可以得到兩電極的電位差值。見右圖。 其中工作電極能對被測離子有響應,電極電位隨離子濃度而變化,而基準電極對任何離子無響應,電極-電位對離子濃度變化保持不變。酸度計用的工作電極(指示電極)為玻璃膜氫離子選擇電極,對 變化敏感,專門檢測溶液中濃度的變化,內有金屬內參比電極(Ag-AgCl)和內參比液;參比電極(外參比電極),與被測離子濃度無關,提供不變的參考電位的電極,由甘汞電極由Hg2Cl2-Hg2和外參比液飽和KCl溶液組成,其中KCl溶液測量時要保證滲出,使鹽橋暢通。現在實驗室常用的電極為復合電極,使用方便。 | 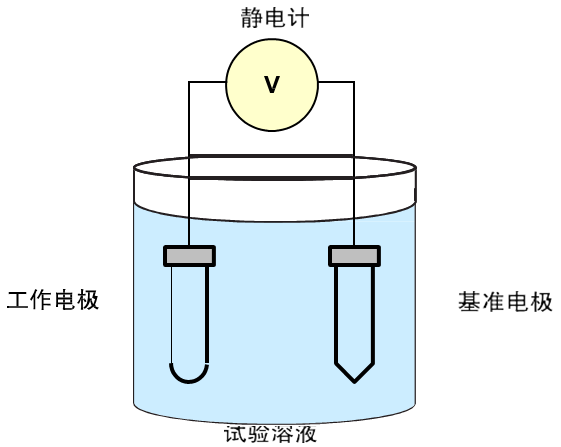 |
由于測得的玻璃電極電位與溶液的pH成正比關系,我們可以通過下列數學關系式求出pH值:
![]()
版權聲明:本資料屬于北京海洋興業科技有限公司所有,如需轉載,請注明出處!




